
Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 36
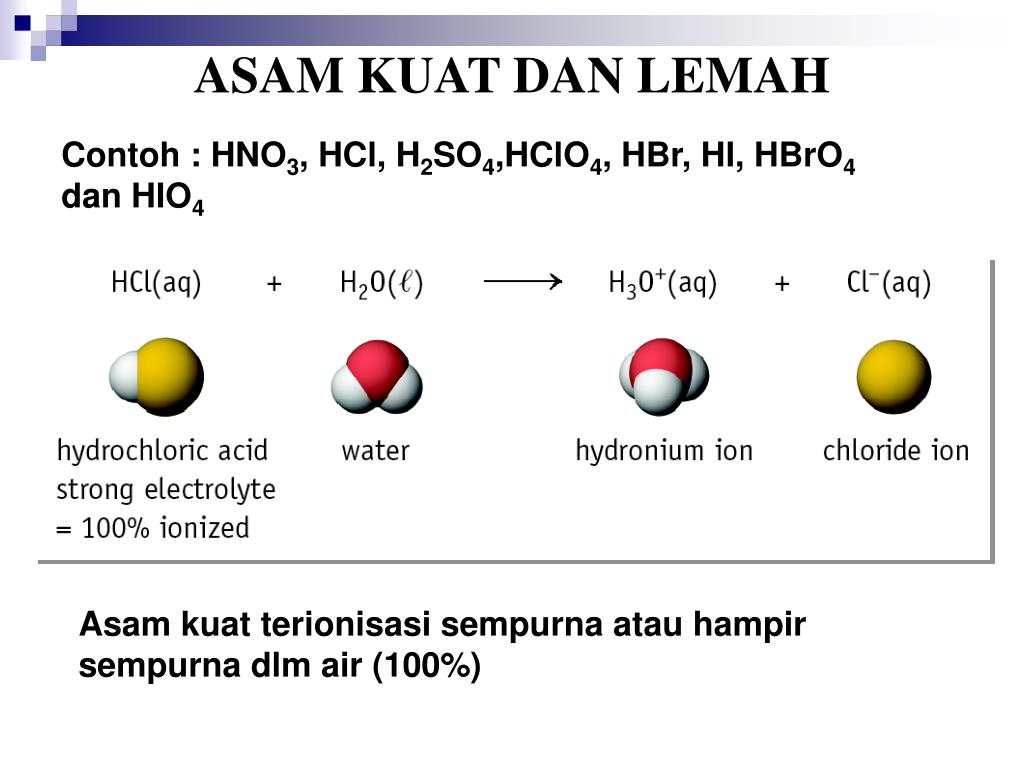
khanacademy.org (1) Asam kuat HCl yang terdisosiasi secara sempurna dalam air dan (2) asam lemah HF yang tidak terdisosiasi secara sempurna dalam air Contoh asam kuat adalah asam klorida (HCl), asam bromide (HBr), asam iodida (HI), asam nitrat (HNO3), dan asam sulfat (H2SO4).

Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah
Asam iodida. Kecuali dinyatakan lain, data di atas berlaku pada suhu dan tekanan standar (25 °C [77 °F], 100 kPa). Asam iodida adalah larutan berair dari hidrogen iodida (HI). Ia adalah sebuah asam kuat, yaitu asam yang ter ionisasi sepenuhnya dalam larutan berair. Ia tidak memiliki warna.

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 21
Misalnya, HCl dan HI keduanya adalah asam kuat, 100% terionisasi dalam air untuk memberikan konstituen ionik masing-masing. Namun, HI lebih kuat daripada HCl. Ini karena jari-jari atom sebuah atom yodium jauh lebih besar daripada jari-jari atom klorin. Akibatnya, muatan negatif pada anion I - tersebar di awan elektron yang lebih besar dan.
Contoh Garam Dari Asam Kuat Dan Basa Kuat Berbagai Contoh
Hidrogen iodida ( H I) adalah suatu molekul diatomik dan hidrogen halida. Larutan berair dari HI dikenal sebagai asam iodida, suatu asam kuat. Hidrogen iodida dan asam iodida adalah, namun, berbeda lantaran hidrogen iodida berbentuk gas dalam keadaan standar, sementara asam iodida adalah larutan berair dari gas tersebut.

Menghitung pH Bagian 4 (pH Asam Kuat) Materi Larutan Asam Basa Kimia SMA Pojan.id YouTube
Contoh Asam Kuat. Berikut contoh-contoh asam kuat, seperti dikutip di buku Asam, Basa, dan Garam oleh Ratna Rima Melati, di antaranya yaitu: 1. Asam Klorida (HCl) Fungsi dari asam klorida, di antaranya sebagai berikut: Pembersih besi dari karat. Bahan pembersih keramik.

Menghitung PH Larutan Garam Asam Kuat Basa Lemah Tyaa
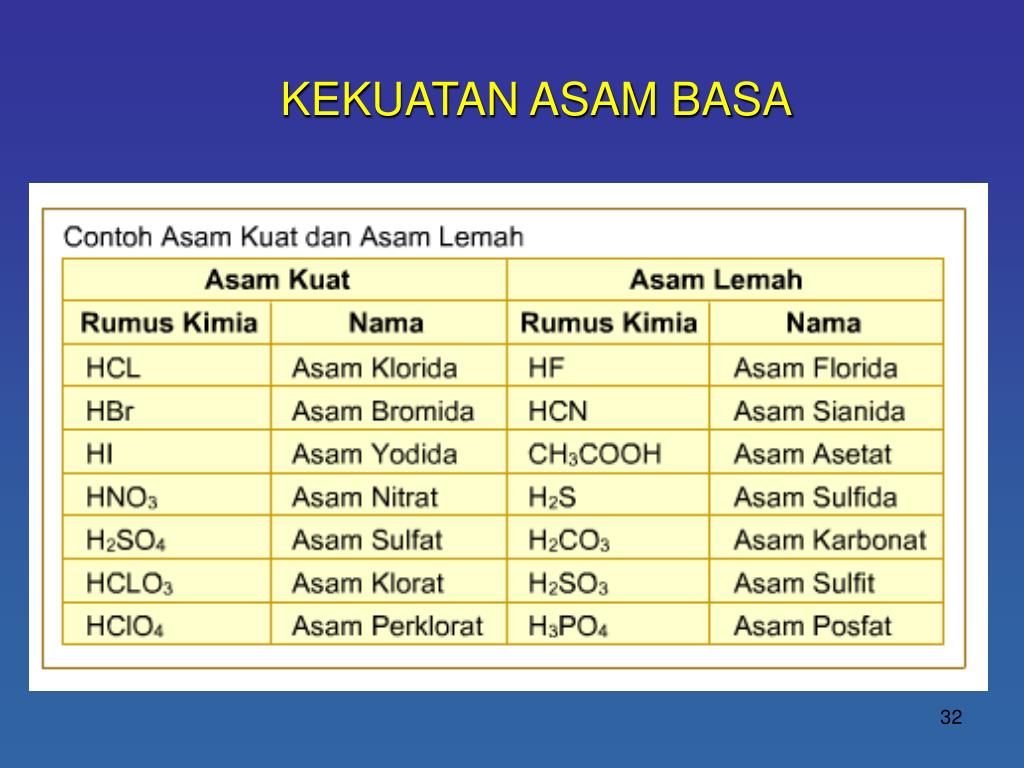
Ada sangat sedikit asam kuat, jadi salah satu cara termudah untuk membedakan asam kuat dan asam lemah adalah dengan mengingat daftar singkat asam kuat. Menu. Rumah. Sains, Teknologi, Matematika. HI - asam hidroiodik; HClO 4 - asam perklorat; HClO 3 - asam klorat; Contoh reaksi ionisasi antara lain: HCl → H + + Cl -HNO 3 → H + + NO 3 -

Cara mudah mencari pH Asam kuat soal fisika SMA YouTube
Buku Interaksi Alam Basa Dalam Kehidupan menulis, menurut sumber asalnya, asam dibedakan menjadi 2 yakni asam organik dan asam anorganik. - Asam organik Asam organik merupakan asam yang banyak terdapat pada bahan makanan yang disebut asam karboksilat, dengan kandungan ikatan C - H atau C - O. Asam ini juga kerap dipakai untuk campuran bahan kosmetik.

Contoh Soal Dan Jawaban Asam Basa Kuat Ruang Belajar
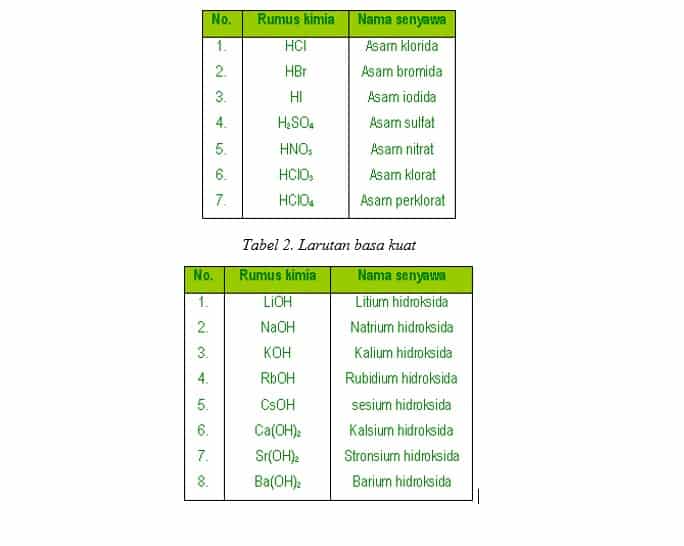
Beberapa contoh asam kuat di antaranya: Asam nitrat (HNO3) Asam hidrogen iodida (HI) Asam klorida (HCl) Asam perklorat (HClO4) Asam bromida (HBr) Asam sulfat (H2SO4) Asam klorat (HClO3) Sementara itu, basa kuat merupakan senyawa basa yang dapat dengan mudah melepaskan ion OH- di dalam air dan dalam larutannya terjadi disosiasi total.
PPT ASAM DAN BASA PowerPoint Presentation, free download ID1244635
Berikut adalah daftar nama asam kuat: Asam klorida (HCl) Asam nitrat (HNO3) Asam sulfat (H2SO4) Asam klorat (HClO3) Asam perklorat (HClO4) Asam bromida (HBr) Asam hidrogen iodida (HI) Baca juga: Hujan Asam: Penyebab, Proses, Dampak, dan Cara Mencegahnya.
Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Berbagai Contoh
Contoh dari asam kuat seperti asam klorida (HCl), asam nitrat (HNO3), asam sulfat (H2SO4), asam bromida (HBr), asam iodida (HI). Basa kuat adalah basa yang juga dapat terionisasi sempurna di dalam air (a=1). Contoh dari basa kuat seperti natrium hidroksida (NaOH), litium hidroksida (LiOH), kalium hidroksida (KOH), barium hidroksida (Ba(OH)2.

Daftar Asam Basa Kuat Dan Lemah
HI - asam hidroiodik; HClO 4 - asam perklorat; Asam Terkuat di Dunia. Meskipun ini adalah daftar asam kuat, mungkin ditemukan di setiap teks kimia, tidak satu pun dari asam ini yang memegang gelar Asam Terkuat di Dunia . Pemegang rekor dulunya adalah asam fluorosulfat (HFSO 3),.

Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah
Lavoisier mendefinisikan asam sebagai zat mengandung oksigen karena pengetahuannya akan asam kuat hanya terbatas pada asam-asam okso dan karena ia tidak mengetahui komposisi sesungguhnya dari asam-asam halida, HCl, HBr, dan HI. Lavoisier-lah yang memberi nama oksigen dari kata bahasa Yunani yang berarti "pembentuk asam".

Cara Praktis Menghitung pH Asam Kuat Hasil Pengenceran YouTube
Kekuatan asam merujuk pada kecenderungan suatu asam, disimbolkan dengan rumus kimia HA, mengalami disosiasi menjadi proton, H +, dan sebuah anion, A −.Asam kuat dalam larutan mengalami disosiasi sempurna, kecuali dalam keadaan pekatnya. + + Contoh asam kuat adalah asam klorida (HCl), asam perklorat (HClO 4), asam nitrat (HNO 3) dan asam sulfat (H 2 SO 4).. Asam lemah hanya terdisosiasi.
Dunia Dalam Berita Tentang Hno3 Asam Kuat Atau Lemah Trending
Cara Membedakan Asam dan Basa. Senyawa asam dapat dengan mudah ditemukan pada buah-buahan, seperti jeruk dan lemon. Selain itu, bisa juga ditemukan pada bahan makanan, seperti cuka. Bahkan, senyawa asam juga banyak digunakan sebagai bahan pengawet makanan lho, misalnya asam benzoat yang dimanfaatkan sebagai pengawet jus buah dan selai.

Detail Contoh Asam Kuat Asam Lemah Basa Kuat Basa Lemah Koleksi Nomer 34
Asam iodida memiliki rumus kimia HI adalah asam kuat yang sangat korosif dan merupakan agen pereduksi yang kuat. HI digunakan sebagai katalis untuk mempercepat reaksi kimia, desinfektan untuk membunuh kumah, dan produksi berbagai macam obat. Asam Sulfat (H2SO4) Asam sulfat digunakan sebagai larutan dalam baterai aki (accu), pembuatan pupuk.

Cara Menghitung Ph Larutan Asam Kuat Dan Asam Lemah Panduan Kimia Riset Sexiz Pix
adjar.id - Tahukah Adjarian apa itu asam kuat dan asam lemah? Asam adalah salah satu jenis larutan yang banyak digunakan dalam kehidupan sehari-hari.. Asam merupakan jenis larutan yang memiliki pH di bawah tujuh. O iya, berdasarkan teori asam-basa bronsted-lowry, asam adalah zat yang mendonorkan proton (H+).. Nah, ada asam yang bersifat kuat, dan ada pula yang lemah.