
Soal Laju Reaksi yang berhubungan dengan persamaan reaksi (m r s) YouTube
Dibaca Normal 4 menit. Berikut ini rangkuman materi tentang konsep laju reaksi rumus dan contoh soalnya. tirto.id - Laju reaksi adalah laju berkurangnya kosentrasi pereaksi atau laju bertambahnya konsentrasi hasil reaksi tiap satuan waktu. Secara sederhana, laju reaksi diartikan sebagai perubahan konsentrasi pereaksi (reaktan) atau reaksi.

Pengertian dan Teori Laju Reaksi Materi Kimia Kelas 11
Untuk cara memahami profil diagram energi aktivasi yang dikaitkan dengan laju reaksi dapat dibaca di sini. Berikut ini beberapa grafik yang paling sering digunakan pada soal-soal ujian nasional maupun ujian lain. Ketika satu pereaksi, misal [A] diubah konsentrasinya maka laju reaksi juga berubah berbanding lurus terhadap perubahan konsentrasi.
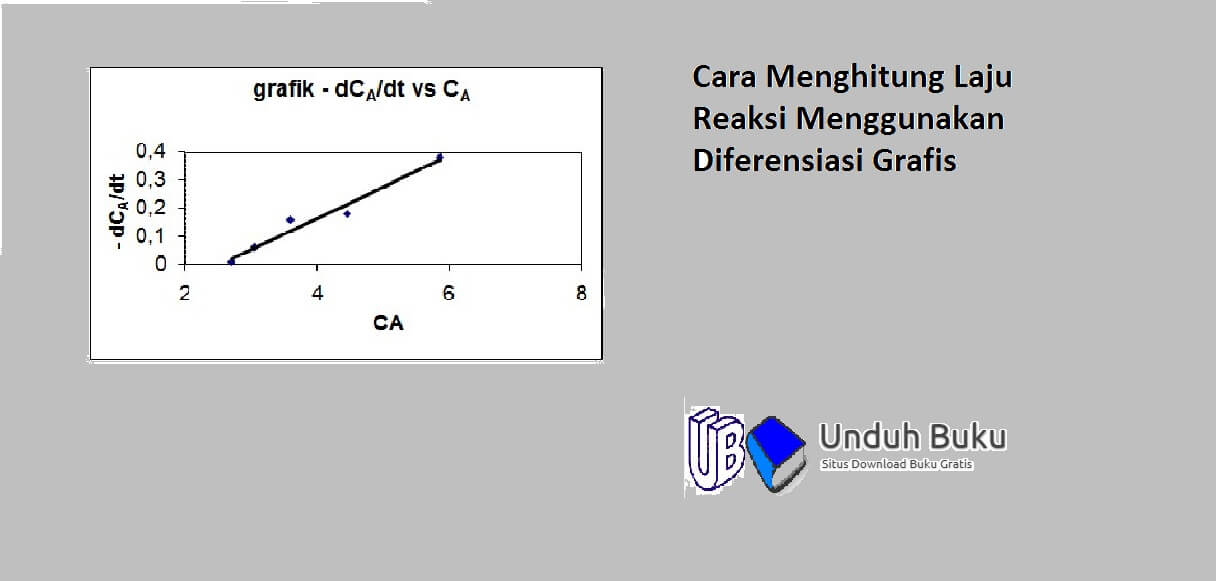
Cara Menghitung Laju Reaksi Menggunakan Diferensiasi Grafis
Pengertian Laju Reaksi. Laju reaksi adalah perubahan konsentrasi dari reaktan ataupun produk per satu satuan waktu. Untuk reaksi dengan reaktan A dan B menghasilkan produk C dan D seperti pada rumus persamaan reaksi berikut, seiring waktu jumlah molekul reaktan A dan B akan berkurang dan jumlah molekul produk C dan D akan bertambah, dan rumus laju reaksi (v) yaitu:

Belajar Kimia Materi dan Contoh Soal Laju Reaksi Part 2 YouTube
Oleh karena itu persamaan dari materi ini adalah sebagai berikut. Di mana, v= laju reaksi (mol/L/s); = perubahan mol; = perubahan waktu. Di mana, v= Laju reaksi (mol/L/s) ; k= konstanta laju reaksi; n= orde reaksi zat B; m= orde reaksi zat A. Secara logika, pada saat bereaksi, zat reaktan pasti makin berkurang, dan zat produk pasti bertambah bukan?

CARA MENENTUKAN ORDE REAKSI DAN PERSAMAAN LAJU REAKSI JIKA DATA YANG DIKETAHUI WAKTU YouTube
Semangat pagi.Di Vidio ini, kita akan belajar cara mudah menentukan persamaan laju reaksi dan orde reaksi.jadi, untuk menentukan persamaan laju reaksi dan.

Cara Cepat menentukan Laju Reaksi Konsep Dasar tabel MTS YouTube
Maka diperoleh bahwa orde reaksi Natrium monoksida (NO) adalah 2 dan orde reaksi bromin (Br2) adalah 1. Tentukan tetapan persamaan laju reaksi Nitrosil bromida (NOBr2) menggunakan data percobaan yang pertama: Jadi, kecepatan laju reaksi pembentukan Bromin adalah sebesar 6 molar per detik. Hal ini berarti pada reaksi antara Natrium monoksida dan.

Persamaan laju reaksi orde reaksi Kimia SMA YouTube
Menentukan Persamaan Laju Reaksi. Persamaan laju suatu reaksi tidak memiliki hubungan dengan stoikiometri reaksi, tetapi ditentukan melalui percobaan, salah satu metode yang sering digunakan adalah metode laju awal. Menurut cara ini, laju diukur pada awal reaksi dengan konsentrasi yang berbeda-beda. Sebagai contoh pada reaksi antara HCl dan.

Contoh Soal Laju Reaksi YouTube
Laju reaksi adalah perubahan konsentrasi reaktan atau produk per satuan waktu. Besaran laju reaksi dilihat dari ukuran cepat lambatnya suatu reaksi kimia. Laju reaksi mempunyai satuan M/s (Molar per detik ). [1] Laju reaksi dilambangkan dengan v atau r. Laju reaksi atau kecepatan reaksi menyatakan bahwa banyaknya reaksi kimia yang berlangsung.

Laju Reaksi [Hubungan Konsentrasi Reaktan dan Waktu] CEK DESKRIPSI YouTube
Semakin cepat reaksi berlangsung, maka harga tetapan laju reaksi semakin besar. Dan berbanding lurus dengan perubahan suhu. Semakin tinggi suhu reaksi, semakin besar harga tetapan laju reaksinya. Cara menentukan tetapan laju reaksi dapat dilakukan setelah diketahui orde reaksi. Untuk lebih mudahnya perhatikan contoh soal berikut.

Persamaan Laju Reaksi dan grafik orde Konsep Mudah YouTube
Laju reaksi adalah laju berkurangnya jumlah reaktan atau laju bertambahnya jumlah produk dalam satuan waktu. persamaan rumus orde faktor soal.. Mencari orde B (n) dengan membandingkan konsentrasi A yang sama, yaitu data 1 dan 2. ½ = 1 . 1 . [½] n, karena k 1 = k 2 = k 3. ½ = [½] n.

CARA MENENTUKAN ORDE REAKSI DAN PERSAMAAN LAJU REAKSI JIKA DATA ADA YANG TIDAK SAMA YouTube
Istilah ini lebih dikenal sebagai laju reaksi. Bagaimana cara mencari laju reaksi itu? Pada artikel ini, Quipper Blog akan membahas beberapa contoh soal terkait laju reaksi. Yuk, simak selengkapnya! Contoh Soal 1. Sebanyak 22,2 gram CaCl2 dilarutkan ke dalam 4 liter air. Molaritas CaCl2 tersebut adalah.. (Ar Ca = 40, Ar Cl = 35,5) 0,05 M;

Cara mudah mencari laju reaksi soal persen yang bereaksi kimia SMA YouTube
2. Orde Satu. Orde reaksi 1 atau suatu reaksi orde satu terhadap salah satu pereaksinya jika laju reaksinya berbanding lurus dengan konsentrasi pereaksi itu. Sebagai contoh bila konsentrasi pereaksi dilipat-duakan, maka laju reaksi akan menjadi kali lipatnya. Bila diplot akan terbentuk kurva berikut: 3.

Laju Reaksi Pembentukan Gas Hidrogen YouTube
A. Faktor Laju Reaksi. Menurut Modul Kimia Kelas 11 oleh Kementerian Pendidikan dan Kebudayaan, laju reaksi dipengaruhi oleh 4 faktor yaitu luas permukaan bidang sentuh, konsentrasi, kenaikan suhu, dan katalis. Simak penjelasannya di bawah ini. 1. Luas permukaan bidang sentuh. Kecepatan reaksi dipengaruhi oleh ukuran partikel zat.

persamaan laju reaksi, UN kimia 2016 pembahasan 024 YouTube
Bagaimana cara mencari laju reaksi jika diketahui waktu? Untuk menjawab pertanyaan tersebut. Terlebih dulu kita perhatikan contoh soal laju reaksi berikut. Dari reaksi H2 dan NO diperoleh data sebagai berikut. [H2]awal (M) [NO]awal (M) Waktu (detik) 0,1 0,1 80 0,2 0,1 40 0,2 0,2 10 Tentukan persamaan laju reaksi! Pembahasan: Hal yang harus kita lakukan

Laju Reaksi Kimia Kelas 11 • Part 5 Persamaan Laju Reaksi dan Orde Reaksi YouTube
Faktor yang Memengaruhi Laju Reaksi. Laju reaksi bisa dipengaruhi oleh beberapa faktor, lho! Faktor-faktor tersebut dapat mempercepat laju reaksi atau malah memperlambat laju reaksi. Faktor-faktor tersebut antara lain suhu, konsentrasi, katalisator, dan luas permukaan sentuh. Nah, kita akan bahas beberapa saja, ya.

CARA MENCARI ORDE REAKSI DAN PERSAMAAN LAJU REAKSI JIKA DATA PERCOBAAN TIDAK ADA YANG SAMA !!
Rumus dan cara mudah menentukan laju pembentukan dan laju penguraian jika diketahui mol awal dan mol pada saat setimbang serta volume . kimia sma.