
Rumus Praktis Hukum Faraday Pojok Kimia
Video penjelasan Hukum Faraday I dan II, contoh soal hukum Faraday (stoikiometri elektrolisis) dan pembahasannya. Materi Elektrolisis kimia kelas 12.#HukumFa.

Apa Bunyi Hukum Faraday 1 dan 2? Kimia Kelas 12
Hukum Faraday II. Dilansir Sampoerna Academy hukum ini dapat digunakan pada dua sel elektrolisis yang mempunyai zat berbeda. Jumlah zat produk elektrolisis yang berbeda akan menghasilkan perbandingan lurus dengan massa ekivalen zat-zat tersebut. Hal ini sesuai dengan bunyi Hukum Faraday II. Melansir dari Vedantu, Hukum Faraday II menjelaskan bahwa massa suatu zat yang disimpan pada elektroda.

Hukum Lenz, Hukum faraday, GGL induksi dan Arus induksi induksi FISIKA
Hukum Faraday dibagi menjadi dua, yaitu Hukum Faraday 1 dan 2. 1. Hukum I Faraday. Hukum I Faraday berbunyi "Total zat yang dihasilkan pada elektroda, berbanding lurus dengan total muatan listrik yang mengalir melalui sel elektrolisis.". Secara matematis dirumuskan sebagai: m = eF atau m = e.i.t/F. Keterangan:

Hukum Faraday 2 Elektrolisis Seri Kimia SMA Kelas 3 YouTube
Hukum Faraday II. Hukum Faraday II memiliki poin yang sangat menarik, di mana hukum ini berlaku pada dua sel elektrolisis dengan kepemilikan zat berbeda. Adanya jumlah zet produk elektrolisis yang berbeda sehingga memunculkan berbanding lurus dengan massa ekuivalen dari zat-zat yang ada tersebut, dalam memahami hal ini sesuai dengan bunyi hukum.

PPT HUKUM INDUKSI FARADAY PowerPoint Presentation, free download ID5738336
Mari kita lihat kembali Hukum Faraday 1 dan Hukum Faraday 2: Hukum Faraday 1 : w ≈ I x t Hukum Faraday 2 : w ≈ ME Jika digabungkan, kita peroleh w ≈ I x t x ME. Perbandingan ini menjadi persamaan dengan penambahan faktor 1/96.500, sehingga diperoleh rumus hukum faraday:. w = 1/96.500 x I x t x ME

Elektrolisis bagian 3. HUKUM FARADAY 2 YouTube
Hukum Faraday II. Berbeda dengan hukum yang pertama, Faraday's Law II menjadi lebih menarik karena berlaku pada 2 sel elektrolisis dengan zat yang berbeda. Perbedaan jumlah dari 2 zat yang berbeda akan menyebabkan massa ekuivalen berbanding lurus dengan zat-zat tersebut.

Foto Hukum Faraday I dan II tentang Elektrolisis Halaman 1
Hukum Faraday II "Massa zat yang dihasilkan pada suatu elektrode selama elektrolisis (G) berbanding lurus dengan massa ekivalen zat tersebut (M ek )." Secara matematis , hukum Faraday II dapat ditulis dalam persamaan berikut.
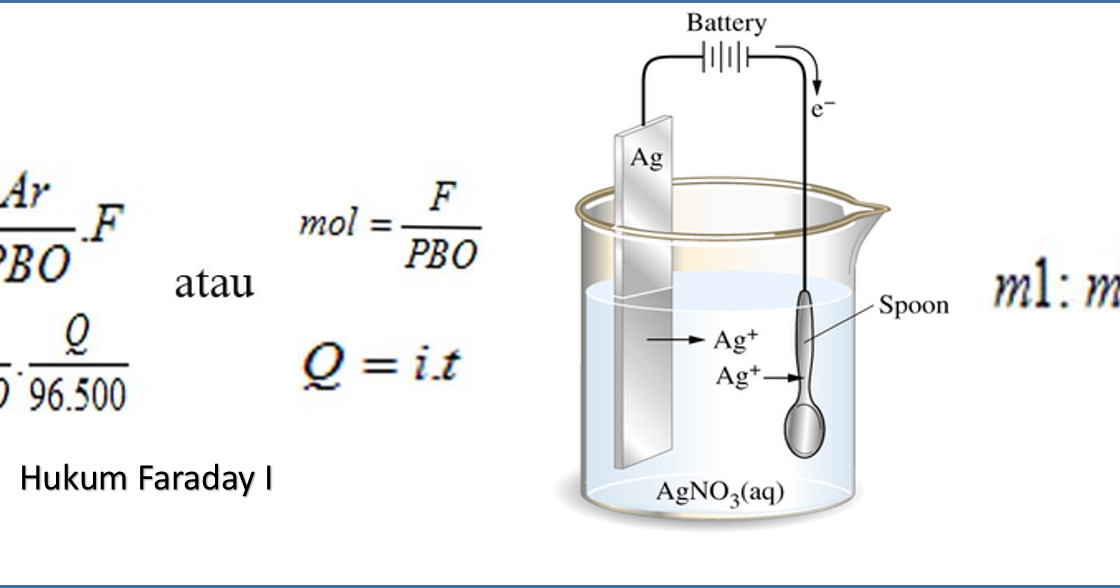
Hukum Faraday Semua Ada
Hukum Faraday: Bunyi, Rumus, & Contoh Soal. Oktober 2, 2023 Oleh Eka, S.Si. Hukum Faraday adalah ilmu yang mempelajari mengenai dasar elektromagnetisme yang merupakan proses perubahan kimia menghasilkan arus listrik maupun sebaliknya. Hukum ini dikemukakan oleh Michael Faraday, seorang ilmuwan asal Inggris yang bekerja dalam bidang elektrolisis.

Hukum Faraday II kelas 12 IPA 2 (SMA DPA) YouTube
Michael Faraday, ia adalah seorang ilmuan asal Inggris yang lahir pada 22 September 1791 di Newington Butts, Inggris. Kemudian ia dijuluki sebagai "bapak listrik", berkat usahanya listrik bisa jadi teknologi yang memiliki banyak kegunaan. Michael Faraday menjadi seorang ahli kimia dan fisika berkat mempelajari aspek kuantitatif dan.

Rumus Hukum Faraday Bentuk turunan II YouTube
Hukum Faraday II menyatakan bahwa "Massa zat yang dihasilkan pada suatu elektroda selama elektrolisis (W) berbanding lurus dengan massa ekivalen (e) zat tersebut." Oleh karena itu, jika beberapa sel elektrolisis disusun secara seri atau arus listrik sama (jumlah muatan listrik yang sama juga), maka perbandingan massa zat-zat yang dihasilkan.
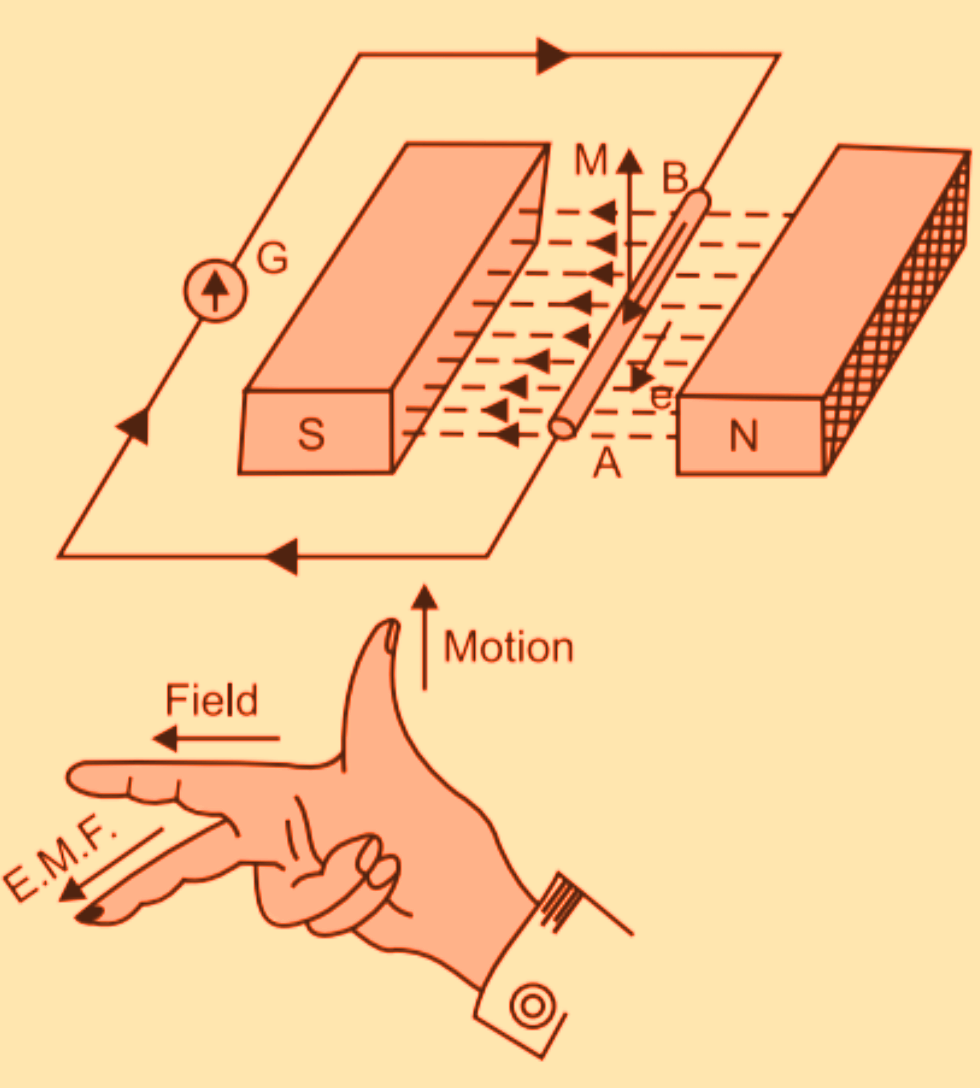
faraday law of induction
Hukum Faraday II. Hukum Faraday II berbunyi: "massa zat yang dihasilkan pada suatu elektrode selama elektrolisis berbanding lurus dengan massa ekivalen zat tersebut." Secara sistematis, Hukum Faraday II dapat disimpulkan dengan persamaan berikut: Keterangan: w=massa zat (kg) ME=massa ekivalen zat (kg)

PERHITUNGAN SEL ELEKTROLISIS (HUKUM FARADAY 2) YouTube
Rumus Hukum Faraday 2 "Massa zat yang dilepaskan pada elektrolisis berbanding lurus dengan massa ekuivalen zat itu" Berdasarkan bunyi hukum Faraday 2 tersebut, maka rumusnya adalah: Keterangan: ME = massa ekivalen. x = jumlah elektron yang diterima atau dilepaskan. Jika rumus hukum Faraday 1 dan 2 ini digabungkan, maka akan diperoleh rumus.

Hukum Faraday II Tanpa Menghafal Rumus YouTube
Materi sel elektrolisishttps://youtu.be/Eh8jt06Zn-s

√ Materi Hukum Faraday Bunyi, Rumus, Contoh Soal
Video penjelasan Hukum Faraday II dengan contoh soal menentukan massa hasil elektrolisis dari dua larutan yang berbeda dengan jumlah listrik yang sama. Mater.

ElektrolisisHukum Faraday II YouTube
Bunyi hukum Faraday 1 yaitu: "Massa zat yang diperoleh pada elektroda saat proses elektrolisis, sebanding dengan jumlah muatan listrik yang mengalir". Dari bunyi di atas, kita dapat melihat bahwa massa produk (W) yang diendapkan pada elektroda akan semakin banyak selama beriringan dengan peningkatan muatan listrik (Q) yang dipakai, maka W ≈ Q.

LATIHAN SOAL DAN PEMBAHASAN HUKUM FARADAY II ( SEL ELEKTROLISIS) YouTube
Hukum Faraday II. Hukum Faraday kedua berbunyi bahwa total zat yang diperoleh dari arus yang sama di dalam beberapa sel berbeda nilainya akan berbanding lurus terhadap berat ekuivalen dari zat-zat tersebut. Hukum Faraday II apabila dibuat dalam bentuk persamaan seperti berikut ini: m1 : m2 = e1 : e2.