
X.2.f. Ikatan Kovalen Tunggal, Rangkap Dua, dan Rangkap Tiga (Teori) YouTube
Ikatan kovalen nonpolar. Nah, bila dua buah atom atau unsur yang terikat dalam ikatan kovalen memiliki keelektronegatifan yang sama besar, maka tidak akan mengakibatkan pengutuban atau polarisasi muatan.. Sebuah senyawa terjadi ikatan kovalen polar apabila ada perbedaan kelektronegatifan yang mengakibatkan terjadinya pengutuban muatan.
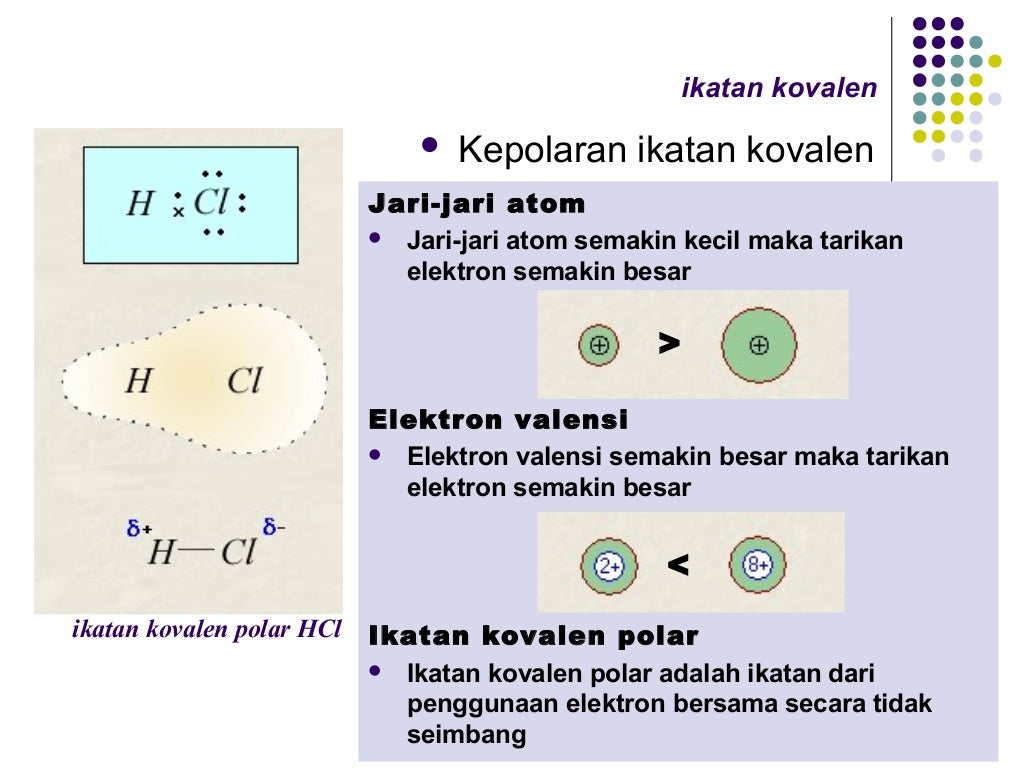
Ikatan kovalen
Ikatan kovalen yang terbentuk pada molekul hidrogen hanya melibatkan satu pasangan elektron atau dua buah elektron, sehingga disebut juga sebagai kovalen tunggal. Contohnya terjadi pada gas fluor dan gas klor. Gas-gas yang kita temukan di alam, seperti hidrogen, nitrogen, oksigen, berada dalam bentuk molekulnya: H 2, N 2, dan O 2. Sebagai atom.

Ikatan Kovalen (Proses Pembentukan Ikatan Kovalen Tunggal, Rangkap 2, Rangkap 3, Kovalen
Ada tiga jenis ikatan Kimia, yaitu ikatan kovalen, ikatan logam dan ikatan ion. Sementara itu, dalam membentuk ion, suatu atom akan melepas atau mengikat elektron. Atom-atom yang mempunyai energi ionisasi rendah, misalnya atom-atom dari unsur golongan IA dan IIA dalam sistem periodik unsur akan mempunyai kecenderungan untuk melepaskan elektronnya.
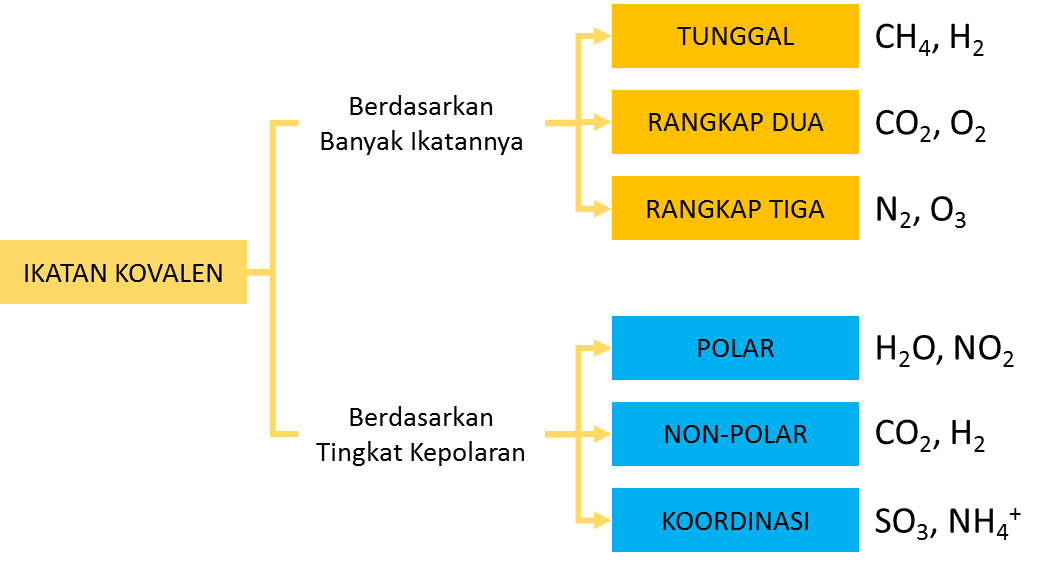
Ikatan Kimia Ikatan Kovalen
Ikatan kovalen adalah ikatan yang terjadi antara dua atau lebih atom non logam dengan pemakaian elektron secara bersama. Kedua atom yang berikatan tersebut akan tertarik pada pasangan elektron yang sama. Contohnya adalah ikatan yang terjadi pada molekul H2. Itulah mengapa ikatan kovalen disebut juga sebagai ikatan molekul.

Ikatan Kovalen KoordinasiKimia Kelas X PestaUli Marbun YouTube
Ikut Bimbel online CoLearn mulai 95.000/bulan.IG CoLearn: @colearn.id https://bit.ly/Instagram-CoLearnSekarang, yuk latihan soal ini!Ikatan kovalen akan terj.

Ikatan Kimia Ikatan Kovalen, Proses Pembentukan Ikatan Kovalen, dan Sifat Senyawa Kovalen
Contoh ikatan kovalen tunggal yaitu terjadi pada H-Cl, CH 4, dan lain lain. Ikatan kovalen rangkap dua; Dalam ikatan kovalen rangkap dua, terdapat dua pasang elektron yang digunakan untuk berikatan sehingga akan membentuk dua ikatan. Satu ikatan yang terbentuk merupakan ikatan sigma seperti pada ikatan kovalen tunggal.
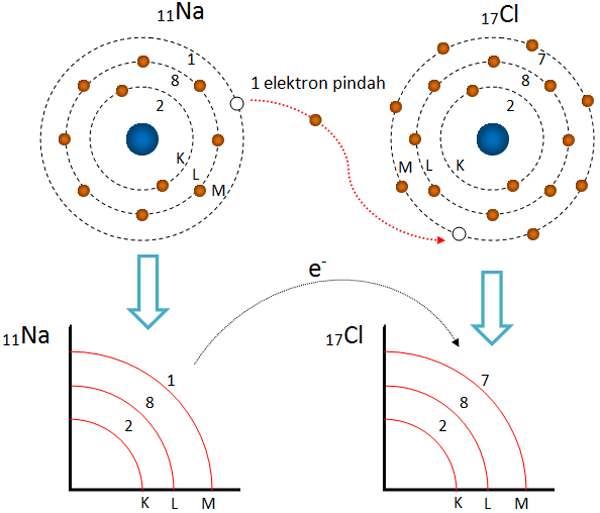
√ Ikatan Kimia (Ikatan Ion, Ikatan Logam, Ikatan Kovalen) Blog Ilmu Pengetahuan
Jenis-Jenis atau Macam-Macam Ikatan Kimia (Ikatan Ion, Ikatan Logam, Ikatan Kovalen) 1. Ikatan Ion. Ikatan ion adalah ikatan yang terbentuk karena adanya gaya tarik menarik secara elektrostatis yang terjadi di antara ion positif dan negatif. Atom yang energi ionisasinya rendah akan mudah membentuk ion positif karena melepaskan elektron.

perbedaan senyawa ion dan kovalen dan contohnya Pippa Poole
Ikatan kovalen yang terjadi antara dua atom yang berbeda disebut ikatan kovalen polar.. Keadaan inilah yang menyebabkan air dalam fasa (bentuk) cair akan mudah berubah menjadi uap air bila dipanaskan sampai sekitar 100 0C, akan tetapi pada suhu ini ikatan kovalen yang ada di dalam molekul H2O tidak putus.

Perbedaan Ikatan Kovalen Dengan Kovalen Koordinasi My XXX Hot Girl
Ikatan kovalen ini dibedakan berdasarkan jumlah pasangan elektron dan kepolarannya. Agar lebih jelas, artikel ini akan membahas seputaran ikatan kovalen, mulai dari pengertian, jenis, sifat, hingga cara menggambar ikatan ini. Yuk, simak pembahasan selengkapnya di bawah ini. Daftar Isi Sembunyikan. Pengertian Ikatan Kovalen.

IKATAN KOVALEN & IKATAN KOVALEN KOORDINASI YouTube
Ikatan kovalen koordinasi merupakan jenis ikatan kovalen yang dapat dibedakan dari sumber elektron dengan penggunaannya bersamaan. Ikatan ini bisa terjadi, jika terdapat satu atom yang menyerahkan pasangan elektron, sehingga atom dari pasangannya tidak akan mampu memberikan elektron. Jenis ikatan ini hanya akan terjadi pada unsur- unsur non logam.
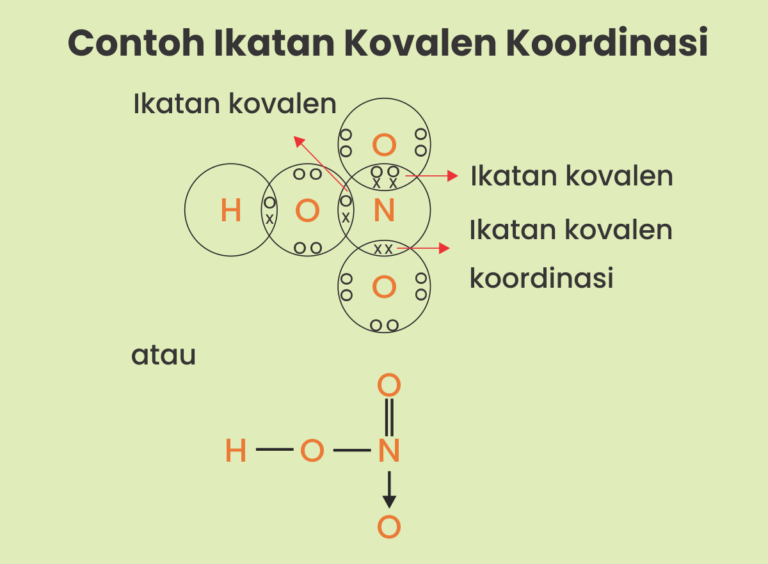
Ikatan Kovalen Nonpolar, Polar dan Koordinasi Siswapedia
Lewat pembahasan ini, kamu bisa belajar mengenai Ikatan Kovalen. kamu akan diajak untuk memahami materi dan tentang metode menyelesaikan soal.. oleh sebab itu ikatan ini paling mungkin terjadi bila atom-atom yang kaya elektron valensi berikatan (unsur golongan 5, 6, 7).
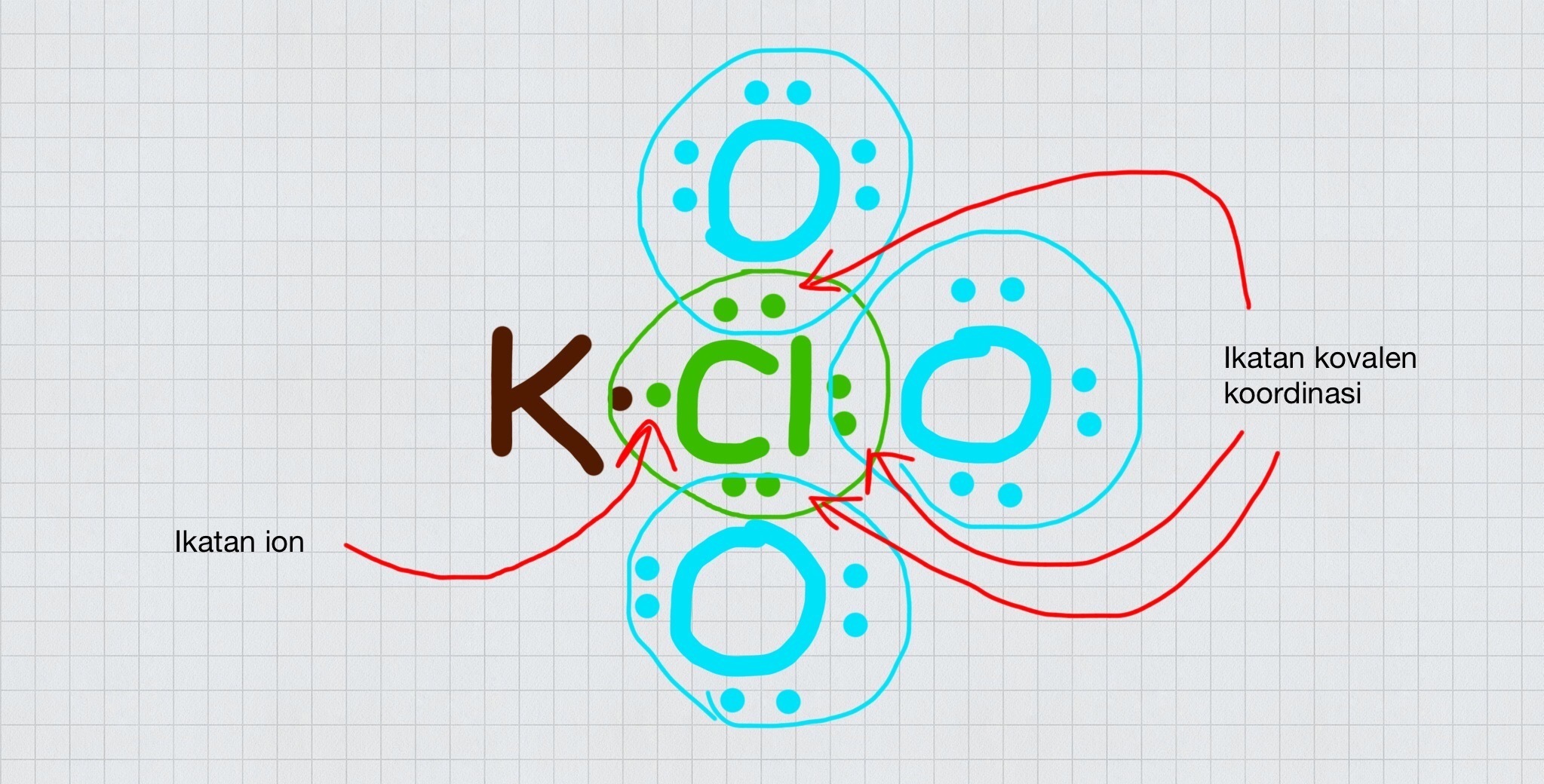
Contoh Soal Essay Ikatan Kovalen Dan Pembahasannya
Polaritas Ikatan Kovalen. Polaritas ikatan kovalen terjadi ketika elektron-elektron dalam ikatan kovalen tidak dibagi secara merata antara kedua atom yang terlibat, yang mengakibatkan terbentuknya muatan parsial positif dan negatif di kedua ujung ikatan tersebut. Hal ini disebabkan oleh perbedaan elektronegativitas antara atom-atom yang terikat.
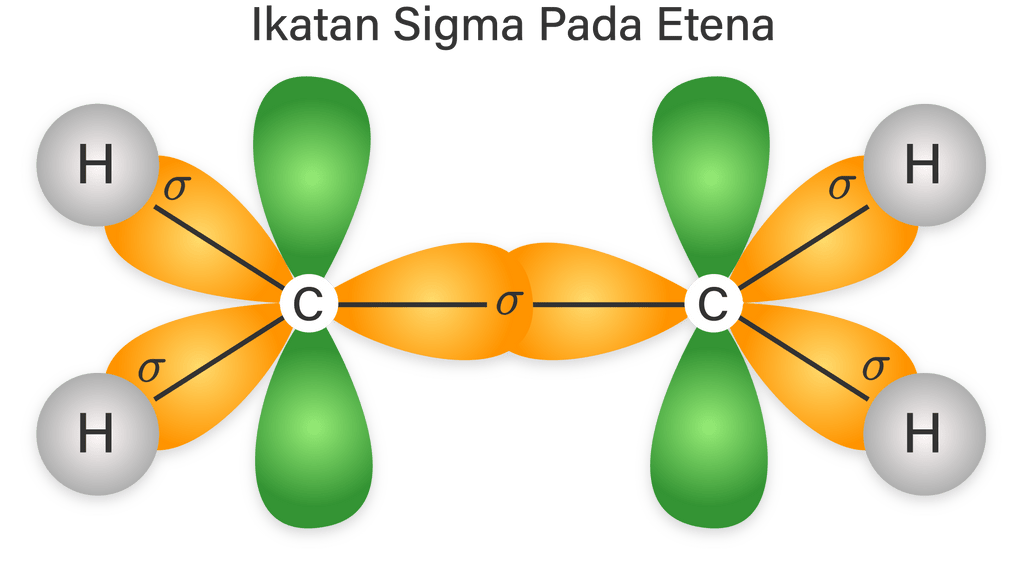
Jelaskan mengapa ikatan kovalen rangkap tiga lebih...
Konsep dari ikatan kovalen yaitu terdapat atom yang sulit melepas atau menerima elektron karena memerlukan atau membebaskan energi yang besar selama proses berlangsung. Baca juga: Gas Mulia: Unsur dan Sifat-sifatnya. Karena kaidah oktet, setiap atom akan berusaha membentuk konfigurasi elektron gas mulia yang lebih stabil, atom-atom ini saling.

Ikatan Kovalen
Contoh ikatan kovalen jenis ini adalah pembentukan senyawa HCl dan CH4. a. Pembentukan HCl. Konfigurasi elektron 1H : 1s1 sehingga elektron valensinya = 1. Untuk mencapai konfigurasi elektron yang stabil (sesuai kaidah duplet) diperlukan 1 elektron. Konfiguarsi elektron 17Cl adalah 1s2 2s2 2p6 3s2 3p5 sehingga CI dan mempunyai elektron valensi = 7.

Molekul Berikut Yang Memiliki Ikatan Kovalen Rangkap 2 Adalah salah satu titik sampel
Jakarta - . Ikatan kovalen adalah ikatan yang terbentuk dari pemakaian bersama pasangan elektron antara dua atom.Pada ikatan kovalen, atom-atom yang terlibat adalah atom-atom non logam. Dijelaskan dalam Smart Book Kimia SMA/MA Kelas X, XI, XII oleh Wikke Yorita Agustin dan Ika Febriana Syafitri, ikatan kovalen terbentuk antara dua atom yang mempunyai elektronegativitas sama atau dua atom yang.
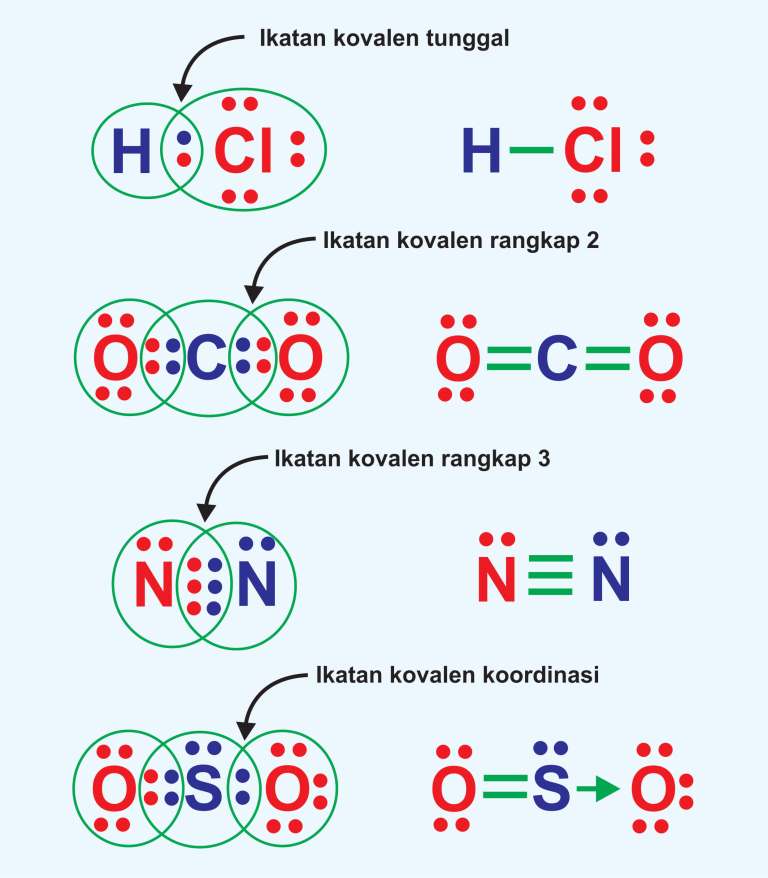
Dasar teori tentang ikatan kovalen
Untuk bisa melihat bagaimana ikatan kovalen terjadi kita harus memahami terlebih dahulu konsep dari struktur Lewis. Oke, kita pahami secara seksama, yuk! Pengertian Struktur Lewis.. Setelah berikatan akan didapatkan 4 pasang elektron ikatan bersama antara atom C dan H, sehingga didapatkan struktur Lewis antara C dan H menjadi seperti berikut