Reaksi Antara Naoh Dan Hclib Freegal Cleveland PELAJARAN
Reaksi indikator PP dengan NaOH pada saat titrasi akan membentuk warna merah muda sebagai titik akhir titrasi. Penelitian ini mengukur kadar sakarin pada seluruh sampel dengan metode titrasi alkalimetri, menunjukkan bahwa terdapat sakarin di dalam sampel. Berdasarkan Permenkes Nomor 722/Menkes/Per/IX/1988.

Larutan 50 mL H3PO4 0,1 M direaksikan dengan 60 mL NaO...
encerkan kembali dengan labu 100 mL. HCl 0,2 N distandarisasi dengan NaOH yang telah distandarisasi dengan H 2 C 2 O 4 2.2.1.3 Larutan standar asam oksalat (C 2 H 2 O 4) Larutan standar asam oksalat 0,2 N dibuat dengan menimbang 1,26 gr asam oksalat (BE = 63) dan dilarutkan dalam labu ukur 100 mL dengan menambahkan aquadest sampai tanda batas.

Reaksi antara asam sulfat dengan aluminium hidroksida aka...
Kesimpulan. Rumus kimia indikator PP adalah C20H13O4N. Indikator PP digunakan untuk menentukan pH suatu larutan dengan cara mengubah warna sesuai dengan pH larutan. Indikator PP memiliki berbagai aplikasi dalam berbagai industri seperti pengolahan makanan, farmasi, dan kosmetik. Meskipun sensitivitasnya rendah terhadap perubahan pH pada kisaran.
Semua Coretan Kuliah Laporan Kimia Dasar I Sifatsifat Unsur
Fenolftalein (bahasa Inggris: phenolphtalein) adalah pewarna yang berperan sebagai indikator pH. Fenolftalein adalah senyawa kimia dengan rumus molekul C 20 H 14 O 4 dan sering ditulis sebagai "HIn" atau "pp" dalam notasi singkat.Fenolftalein sering digunakan sebagai indikator dalam titrasi asam-basa.Untuk aplikasi ini, ia berubah warna dari tak berwarna dalam larutan asam menjadi merah muda.

Bila 20 mL NaOH 1 M direaksikan dengan 16 mL H2 C2 O...
Telah ada artikel sebelumnya yang menjelaskan bahwa ada suatu senyawa yang berfungsi sebagai suatu indikator yang menunjukkan zat bersifat asam dan zat bersifat basa. Salah satu contoh indikator asam-basa yang terkenal adalah indikator phenolphtalein (PP) yang biasanya digunakan dalam praktikum titrasi. Indikator PP ini mempunyai rentang pH 8,0 - 9,6 dengan perubahan warna dari tak…

Jual indikator PP 250 ML Phenolphtalein sol. indicator 1. Merck 107227 Kota Bekasi AHYA
Dimasukkan dalam tidak berwarna NaOH + indikator PP memberikan protein pada basa tabung reaksi -Indikator PP : : larutan berwarna kuat atau menerima protein 2.. tujuan percobaan ini yaitu untuk mengidentifikasi asam amino dengan inti benzene pada sampel protein susu dengan reaksi ksanthoprotein. tes dikatakan positif ditunjukkan dengan warna.

Mari bertanya! Tanya MIPI
Gambar 4.3.1 Penambahan indikator pp pada larutan asam oksalat Gambar 4.3.2 Hasil titrasi asam oksalat dengan NaOH 9 Hasil akhir dari proses titrasi asam oksalat dengan NaOH adalah didapatkan larutan berubah menjadi ungu dan volume NaOH yang digunakan sebanyak 3,5 mL.

f
Percobaan kedua, larutan NaOH 0,05 M di tetesi dengan indikator PP. Warna awal larutan NaOH adalah bening dan setelah di tetesi indikator PP warnannya berubah menjadi merah tua. Ini menunjukan bahwa NaOH bersifat basa karena pada lingkungan basa, indikator PP akan berubah menjadi warna merah.. Hubungannya dengan reaksi redoks, karena reaksi.

Perbandingan koefisien H2O dengan NaOH dalam reaksi redok...
Gambar 2. Kurva Titrasi NaOH Terhadap Volume HCl dengan Menggunakan Ekstrak Metanol Buah Lakum Indikator fenolftalein (pp) digunakan sebagai indikator pembanding dalam proses titrasi basa kuat-asam kuat, hasil yang diperoleh menunjukkan rentang pH yaitu 9,83-4,20 dengan warna merah muda menjadi tidak berwarna. Nilai standar

LENGKAP UNTUK PEMULA ‼️ HIDROLISIS GARAM PART2 ‼️ CARA MENULISKAN REAKSI HIDROLISIS YouTube
Penggaraman berbeda dengan neutralisasi hal ini disebabkan reaksi yang terjadi adalah titrasi asam lemah oleh basa kuat.. + 100 ml Aquadest Larutan baku NaOH 4.1.3 Hasil Standarisasi larutan baku sekunder 25 ml 0,1 N H2C2O4 + 2 NaOH + 3 tetes Indikator pp Na2C2O4 + 2H2O perubahan warna menjadi merah muda Pada titrasi pertama volume NaOH.

Standarisasi NaOH dengan Asam Oksalat Metode Titrasi Asam Basa YouTube
Di bawah ini jenis-jenis indikator asam basa: 1. Kertas Lakmus. Indikator buatan asam basa yang pertama adalah kertas lakmus. Indikator ini yang paling banyak digunakan di laboratorium karena praktis dan harganya cukup murah. Ada dua jenis kertas lakmus yang bisa kamu jumpai, yaitu lakmus merah dan lakmus biru.

Percobaan titrasi antara 10 mL larutan H2SO4 dengan NaOH
Berdasarkan reaksi: 2 NaOH + H 2 C 2 O 4.2H 2 O Na 2 C 2 O 4 + 4 H2O 2. Buat larutan standar asam oksalat: Timbang 0,3 gram asam oksalat dihidrat (H 2 C 2 O 4.2H 2. tambahkan 3 tetes indikator PP, dititrasi dengan larutan NaOH yang telah distandarisasi. Catat volume NaOH yang diperlukan untuk netralisasi asam cuka, yaitu

Laporan Praktikum Standarisasi Larutan NaOH untuk Menentukan Kadar Asam Cuka Perdagangan
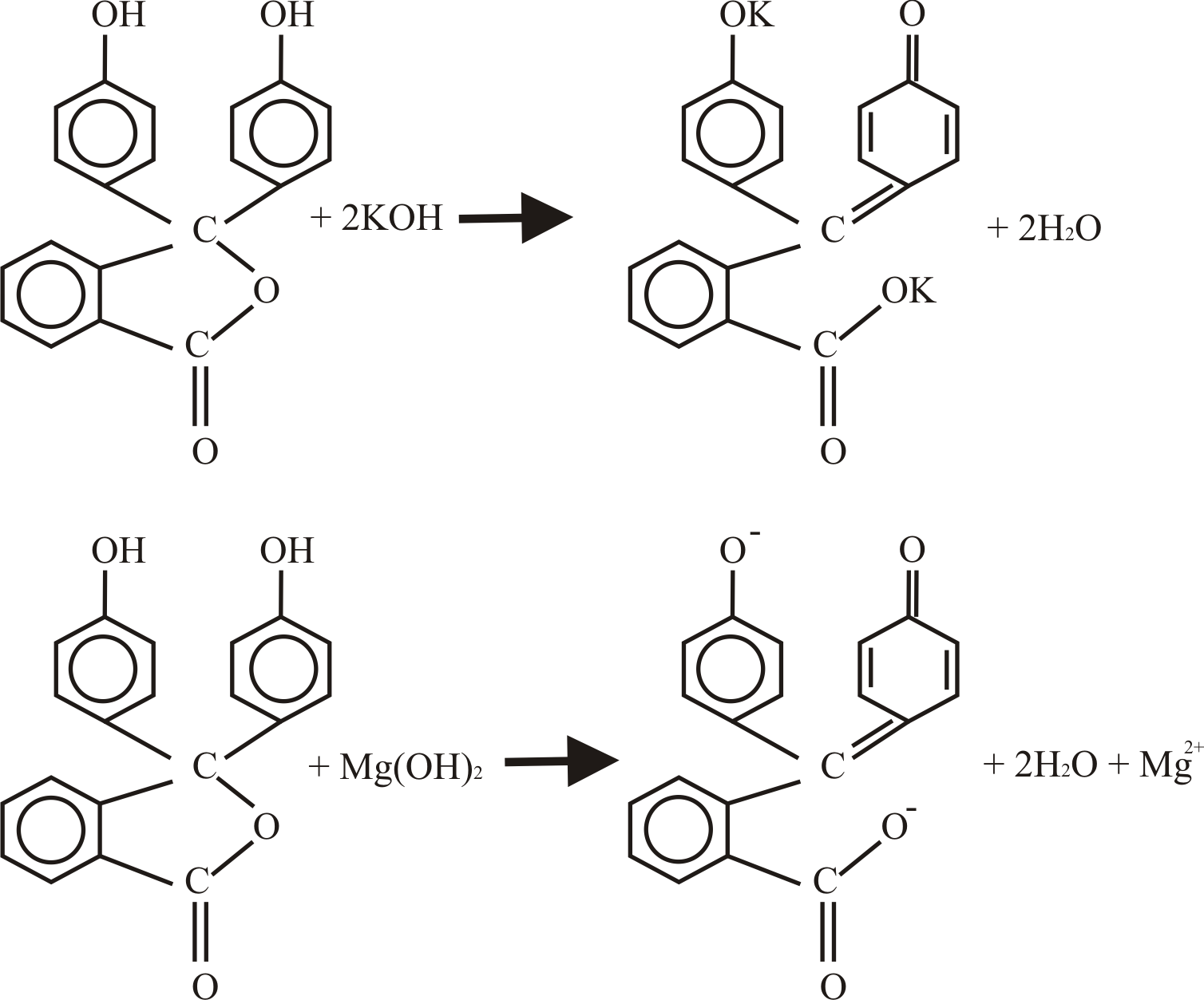
NaOH dengan asam oksalat dilakukan dengan cara titrasi dan indikator yang digunakan yaitu indikator fenolftalein (pp).. Reaksi indikator pp saat bereaksi dengan basa ditampilkan pada gambar.

Sebanyak 50 mL larutan NaOH 1 M direaksikan dengan 100 mL larutan HCl 1 M, maka pH larutan
Reaksi-reaksi 4.2.1. Naoh + Indikator PP - NaOH + PP OH OH ONa O C + NaOH C + 2H2O O C C ONa O O Fenolftalein merah lembayung 9 4.2.2.. Ketika CH3COOH ditetesi dengan indikator PP, warna larutan tidak berubah atau masih bening. Hal ini dikarnakan indikator PP tidak bereaksi dengan asam. Setelah ditetesi dengan NaOH warna larutan menjadi.
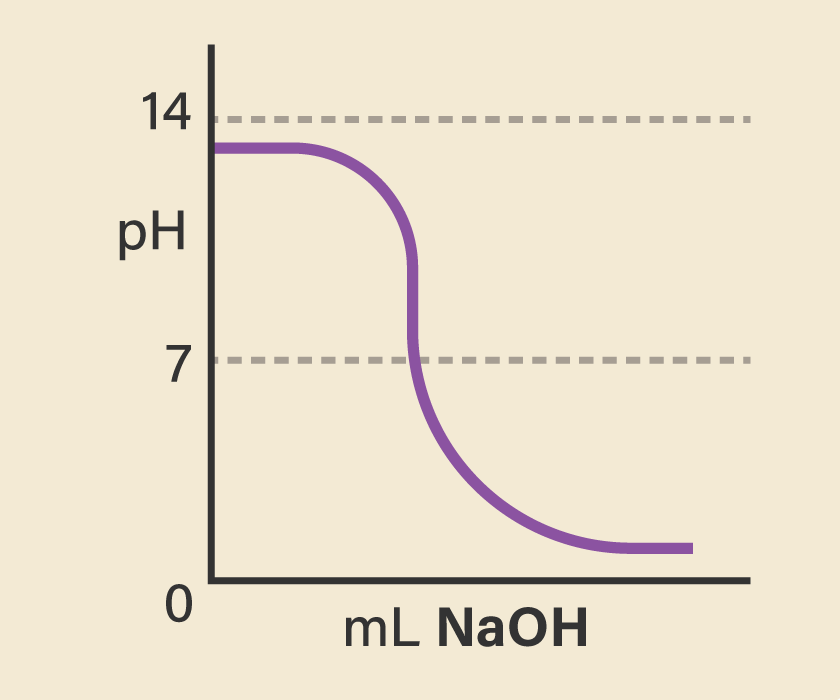
Kurva yang menunjukkan hasil titrasi HCl dan NaOH
Hasil Pengamatan Perlakuan Asidimetri - Dicampurkan 10ml NaOH dan 10ml akuades - Ditetesi Indikator PP 3 tetes - Ditittrasi dengan asam oksalat dehidrat 10,15ml - Dihitung konsentrasi NaOH Alkalimetri - Dimasukkan 10ml asam cuka yang telah diencerkan kedalam tabung reaksi - Ditetesi indikator PP 3 tetes - Dititrasi dengan NaOH 15,5 ml.

Data hasil percobaan titrasi larutan NaOH dengan larutan
Indikator kimia yang biasa digunakan yaitu indikator pp atau phenolptalein. Indikator ini diteteskan sebanyak 1-2 tetes ke dalam titrat. Kalau tidak diteteskan, maka titrat tidak bisa berubah warna, sehingga kita tidak akan tahu kapan titik ekuivalennya terjadi. Baca Juga: Kesetimbangan Kimia, Jenis-Jenis, Persamaan Reaksi, dan Tetapannya