
Sifat Unsur Halogen dan Manfaatnya dalam Kehidupan Seharihari Kimia Kelas 12
Istilah halogen berasal dari bahasa Yunani yang artinya pembentuk garam. Dikutip dari buku Kimia Unsur Golongan Gas Mulia, Halogen, Alkali, dan Alkali Tanah yang disusun oleh Tantri Ambarsari (2020), halogen adalah senyawa yang unsur-unsurnya dapat bereaksi dengan logam untuk membentuk garam. Reaktivitas unsur halogen sangat besar sehingga.

Halogen [Golongan VIIA] Kimia Unsur Kelas 12 YouTube
Kelompok 8 Alkaloid - Copy. BAB I_kimorgnk1. SIFAT PERIODIK. UNSUR HALOGEN SIFAT FISIK SIFAT KIMIA. Memiliki 7 elektron valensi. Atom unsur halogen sangat mudah menerima electron dan membentuk ion negative. Dari atas ke bawah, keelektronegatifan, afinitas electron dan sifat pengoksidasi golongan halogen semakin menurun.

Sifat fisika unsur halogen( golongan VllA) kimia SMA YouTube
Golongan 17 atau Golongan VIIA. Unsur-unsur pada golongan VIIA disebut juga unsur golongan halogen. Semua unsur yang terdapat pada golongan ini termasuk non-logam. 1. Sifat Fisika. Selain itu diketahui pula wujudnya pada suhu ruang: Fluorin : gas berwarna kuning. Klorin : gas berwarna kuning-kehijauan.

Unsur Halogen Pembelajaran Kimia
Berikut sifat-sifat unsur halogen: Afinitas elektron yang tinggi karena unsur halogen lebih mudah membentuk ion negatif. Energi ionisasi halogen tinggi karena unsur halogen sukar melepaskan elektron valensinya menjadi ion positif. Oleh karena itu, di alam tidak ada unsur halogen yang membentuk ion positif, tetapi membentuk ion negatif.
PPT HALOGEN PowerPoint Presentation, free download ID5395334
16. Sifat berikut tidak dimiliki oleh golongan halogen yaitu… a. Unsure bebasnya berbentuk molekul diatomic. b. Titik didih dari atas kebawah semakin besar. c. Merupakan oksidator kuat. d. Mudah bereaksi dengan zat lain. e. Tidak bereaksi dengan air. Jawaban : E. Penyelesaian: Secara umum, sifat kimia unsur-unsur halogen, antara lain sebagai.

Golongan Halogen
Unsur halogen dalam sistem periodik unsur menempati golongan VIIA. Berikut sifat - sifat umum dari unsur halogen: Pada suhu kamar F 2 dan Cl 2 berwujud gas, Br 2 berwujud cair, dan I 2 berwujud padat. Dalam keadaan bebas partikelnya berupa molekul diatomik dan bersifat racun. Ketika bersenyawa memiliki bilangan oksidasi -1, +1, +3, +5, dan +7.
UnsurUnsur Halogen Kimia, Unsur Halogen Karakteristik Tugas Sekolah
Sifat dan Kegunanaan Dari Unsur-Unsur Golongan Halogen (VII A) Halogen adalah enam unsur nonlogam, sangat reaktif di bawah Golongan VII A(kolom 17) dari tabel periodik. Mereka adalah bahan pengoksidasi yang sangat kuat, yang berarti mereka mengambil elektron dari zat lain. Mereka juga sangat reaktif dan biasanya membentuk garam dengan Golongan I A, yaitu logam alkali.

PPT Golongan VII A Unsur Halogen PowerPoint Presentation, free download ID2090544
Halogen sendiri berasal dari bahasa Yunani yang merupakan "unsur yang akan menghasilkan garam jika bereaksi dengan logam". Kalau kita lihat dalam tabel periodik, unsur-unsur yang termasuk ke dalam halogen adalah Fluor (F), klorin (Cl), bromin (Br), Iodin (I), dan Astatin (At). Semua unsur ini, punya sifat racun yang cukup tinggi.

Halogen kimia unsur
Halogen-halogen memiliki beberapa sifat fisik dan kimia yang unik, diantaranya adalah sebagai berikut : Sifat Fisik: Halogen-halogen adalah gas di udara yang tidak memadai, kecuali astat yang merupakan padatan. Fluor dan klor adalah gas yang sangat reaktif dan mudah terbakar. Brom dan jodida adalah gas yang lebih stabil, tetapi masih sangat.
UnsurUnsur Halogen Kimia, Unsur Halogen Karakteristik Tugas Sekolah
Sifat-sifat kimia halogen adalah sebagai berikut: Golongan yang sangat reaktif. Halogen merupakan oksidator kuat. Oleh karena itu mudah mengikat elektron atau mudah tereduksi. Urutan kekuatan oksidator golongan halogen: F 2 > Cl 2 > Br 2 > I 2. Sangat berbahaya terhadap mata dan tenggorokan. Mempunyai bau yang merangsang dan berwarna.

Sistem Periodik Golongan VIIA(Halogen) indonesia version
78 questions. 1. Multiple Choice. Diantara reaksi berikut yang tidak dapat berlangsung adalah. . 2. Multiple Choice. Dari pernyataan di bawah ini yang menunjukkan sifat unsur halogen adalah. . 3. Multiple Choice.

Halogen kimia PETA KONSEP GOLONGAN HALOGEN SIFAT PERIODIK UNSUR HALOGEN SIFAT FISIK SIFAT
45 seconds. 1 pt. Perhatikan Sifat - sifat berikut. 1. dapat bereaksi dengan unsure logam. 2. dengan hidrogen dapat membentuk senyawa yang bersifat asam. 3. elektronegatifitas lebih besar kalau dibandingkan dengan golongan unsur lain. 4. membentuk molekul diatomic. Sifat-sifat unsur halogen adalah…. 1, 2, 3.
UnsurUnsur Halogen Kimia, Unsur Halogen Karakteristik Tugas Sekolah
Halogen adalah nama golongan VIIA pada tabel periodik unsur. Secara umum, sifat-sifat halogen sebagai berikut: Dengan demikian, berdasarkan sifat-sifat halogen di atas, maka semua pilihan pada soal benar.. Jadi, jawaban yang tepat adalah E.

Diantara Sifat Berikut Yang Bukan Merupakan Sifat Unsur Halogen Adalah crossover pasif 2 way
Unsur ini terdiri dari F (fluorin), Cl (klorin), Br (bromin), I (iodin). Dan At (astatin). Karakteristik unik yang perlu elo ingat halogen ini merupakan satu-satunya kelompok unsur dari tabel periodik yang memiliki ketiga keadaan materi yaitu padat, cair dan gas. unsur halogen - arsip zenius.

Sifat dan Kegunaan Dari UnsurUnsur Golongan Halogen (VII A) Sains Kimia
Unsur halogen termasuk golongan. VIIA. Sifat yang tidak dimiliki golongan halogen. Tidak bereaksi dengan air. Diantara unsur-unsur halogen, yaitu fluorin, klorin, bromine, dan iodine. Manakah yang merupakan pengoksidasi terkuat. Iodine. Kecenderungan sifat unsur halogen dari fluorin ke iodine adalah.kecuali. Energi ionisasi makin besar.
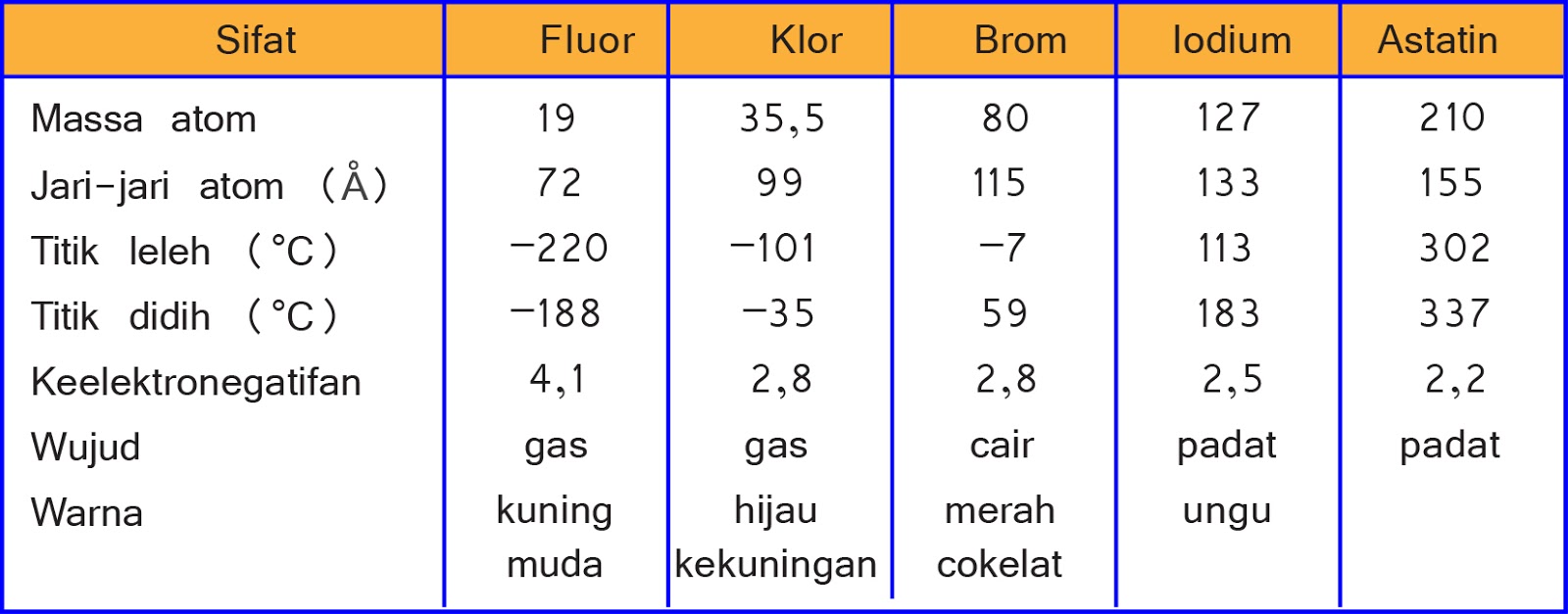
Kimia Kelas 12 Sifat Unsur Halogen Dan Manfaatnya Dalam Kehidupan Riset
Unsur halogen memiliki 1 elektron tidak berpasangan pada orbital p terluarnya. Karena itu, unsur halogen sangat reaktif menangkap 1 elektron dari luar agar stabil. Halida adalah bentuk anionik dari halogen . Halida mempunyai konfigurasi elektron . Beberapa perbedaan antara halogen dan halida ditampilkan pada tabel berikut: